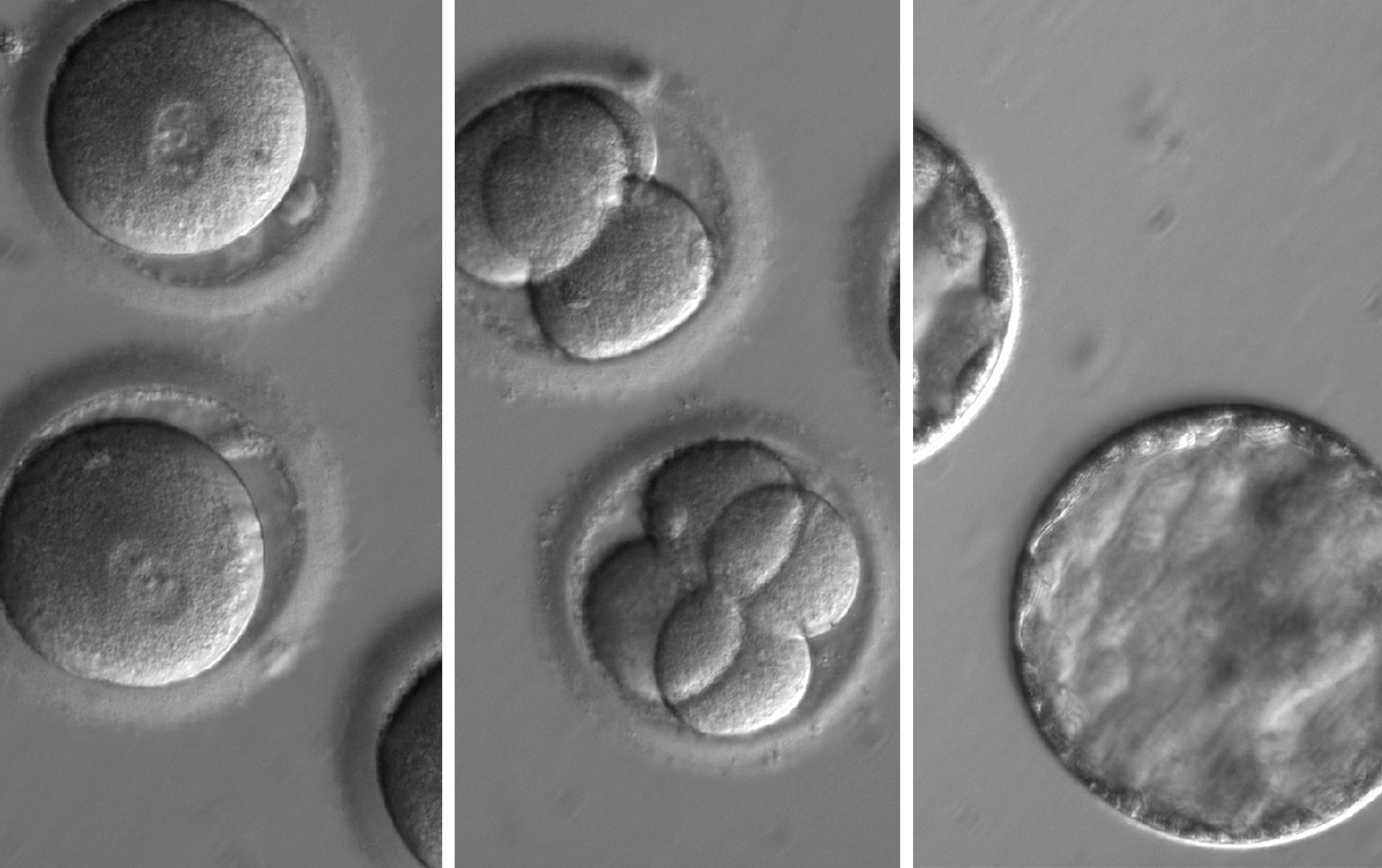
Ante la polémica sobre todo lo relacionado con la edición genética, la investigación revela que algunos embriones no siguieron las instrucciones marcadas por la herramienta de edición sino que cogieron como plantilla el ADN sano de la madre. Este fenómeno podría facilitar la aprobación de nuevas investigaciones
La puerta para crear a las primeras personas modificadas genéticamente se ha abierto: un equipo de científicos estadounidenses ha sentado las bases de las personas de diseño al alterar los genes de decenas de embriones humanos para eliminar un gen relacionado con una enfermedad cardíaca.
El investigador de la Universidad de Salud y Ciencias de Oregón (EEUU) Shoukhrat Mitalipov y su equipo han utilizado con éxito la herramienta de edición de genes CRISPR-Cas9 para corregir un error en el ADN responsable de enfermedades en docenas de embriones humanos en etapas tempranas. Este proyecto de edición de embriones es el más extenso de su clase, y fue descrito por primera vez la semana pasada por MIT Technology Review.
Según un detallado informe publicado en Nature, los científicos han demostrado que es posible corregir una mutación en el gen MYBPC3, el responsable de una enfermedad cardíaca hereditaria mortal, la miocardiopatía hipertrófica.
El procedimiento fue sorprendemente eficaz y podría incluso considerarse como un ensayo clínico, asegura el equipo de científicos. Durante una conferencia telefónica con periodistas, Mitalipov detalló: "Hemos sentado las bases con esta mutación en particular, por lo que probablemente estamos mucho más cerca de poder realizar aplicaciones clínicas. Los ensayos clínicos podrían requerir implantar algunos de estos embriones para establecer un embarazo y monitorizar los nacimientos de los niños; incluso, con suerte, podremos hasta realizar un seguimiento".
Este impresionante avance vuelve a remover el eterno debate sobre si se debe utilizar la tecnología de edición genética para alterar el patrimonio genético humano. El sector crítico se han mostrado preocupado y ha lanzado al aire los riesgos desconocidos que estas modificaciones de los embriones suponen para los niños. Sostienen, además, que sería un camino peligroso hacia los "bebés de diseño" mejorados genéticamente.
La razón médica para hacer la modificación de la línea germinal (es decir, alterar un embrión), es reparar un defecto genético antes del nacimiento para que el rasgo no se transmita a las generaciones futuras. "Esto erradicaría completamente la mutación y la enfermedad de la herencia genética de una familia", dice Mitalipov.
Antes de este experimento, en China se realizaron tres investigaciones sobre edición de genoma en embriones humanos. Pero el trabajo de Mitalipov es mucho más extenso que cualquier investigación previa, con un total de 150 embriones humanos.
En cada caso, los óvulos obtenidos de donantes sanos fueron fertilizados con esperma de un único hombre portador de la mutación cardiomiopatía.
¿Es posible prevenir el cáncer antes del nacimiento? Mitalipov cree que sí. Sostiene que la edición genética podría convertirse en una herramienta preventiva para proteger el riesgo de un recién nacido ante una amplia gama de enfermedades, tumores incluidos. Por ejemplo, CRISPR podría ser inyectado en embriones para arreglar mutaciones en el gen BRCA, asociado con un alto riesgo de cáncer de mama y ovarios.
El debate está servido, pero hay quien tiene una postura muy clara. Algunas personas cuyas familias portan y sufren enfermedades hereditarias no dudarían en emplear la tecnología, si estuviera disponible. Por ejemplo, Lisa Salberg, de 49 años, que fue diagnosticada de la misma afección genética a los 12 años, dice que si tuviera un hijo elegiría la posibilidad de realizar la edición de genes "en un minuto".
Salberg, que es la fundadora de la Asociación de Cardiomiopatía Hipertrófica (HCMA, por sus siglas en inglés), viene de una familia con una herencia genética complicada: su padre tenía la enfermedad y su hija también la heredó. La defensora recuerda. "A los 12 años me dijeron que podía morir de repente y que no había nada que pudiera hacer. Nunca he sabido cómo es sentirse sano".
Los escépticos de la edición de la línea germinal argumentan que la modificación de genes en embriones es innecesaria. Según ellos, las mujeres sometidas a fecundación in vitro (FIV) pueden optar por un diagnóstico genético previo a la implantación, es decir, una prueba realizada en embriones de FIV para determinar si están afectados por una mutación genética.
En el caso del fallo del gen MYBPC3, conocido como trastorno autosómico dominante, la mitad de los embriones de una pareja serían portadores de la enfermedad; la otra mitad, no. Por lo tanto, los doctores podrían hacer un test para saber cuáles están sanos para implantar sólo esos.
La existencia de esta prueba implica que la técnica de edición genética en embriones tiene "una ventana de oportunidad muy estrecha ", dice el investigador del genoma en el Centro Nacional de Biotecnología de Madrid (España) Lluís Montoliu. Este test de diagnóstico de preimplantación fue utilizado aproximadamente en una de cada cuatro mujeres de 35 a 40 años que se sometieron a fecundación in vitro durante el año pasado en Estados Unidos, según cifras de la Sociedad para la Tecnología Reproductiva Asistida. Pero una de las autoras del estudio y profesora de obstetricia y ginecología en la Universidad de Salud y Ciencias de Oregón, Paula Amato, sostiene que reparar los embriones aumentaría el número de nacimientos sanos y que, potencialmente, aceleraría el proceso para embarazos exitosos.
Los investigadores también se dieron cuenta de que la efectividad del proceso aumentaba cuando CRISPR se inyectaba en los ovarios directamente con el esperma. En estos casos, 42 de los 58 embriones resultaron sanos y libres de la mutación de cardiomiopatía hipertrófica. En otras palabras, editar genéticamente con CRISPR aumentó sustancialmente el número de embriones sanos: de un estimado 50% a aproximadamente el 72%. Los 16 embriones restantes sufrieron inserciones o supresiones genéticas no deseadas, lo que demuestra que la técnica de edición aún requiere más mejoras.
Estos avances genéticos con aplicaciones en los primeros años de vida podrían tener otras implicaciones, como generar grandes ahorros para la sociedad y el sistema médico. Por ejemplo, Salberg puede nombrar a seis parientes, entre ellos un tío abuelo de 19 años y una hermana de 36 años, que murieron muy jóvenes por culpa de la enfermedad. En cuanto a ella, ya ha recibido cinco implantes de desfibriladores, ha sufrido un derrame cerebral, ha perdido parte de su visión, y hace seis meses se sometió a un transplante de corazón. La paciente detalla: "Si haces las cuentas, CRISPR sería mucho más barato. Si pudiera volver a 1967 y mi madre tuviera la opción de utilizar la edición genética con CRISPR para eliminar la mutación [de la miocardiopatía hipertrófica], mi vida sería diferente en muchs aspectos".
La cardiomiopatía hipertrófica afecta a una de cada 500 personas, y puede provocar una insuficiencia cardíaca repentina en individuos que aparentemente sanos.
Pero a pesar de estos escenarios, la edición de la línea germinal se topará con grandes desafíos, en particular en los Estados Unidos. Aunque el concepto de los 'bebés a la carta' ha sido defendido para tratar casos extremos, los Institutos Nacionales de Salud no financian investigaciones con embriones humanos, y el Congreso de los Estados Unidos ha prohibido a la Administración de Alimentos y Medicamentos aprobar cualquier ensayo clínico de este tipo.
Mitalipov opina: "Hay un largo camino por delante, sobre todo si se quiere hacer este estudio de manera regulada. En este momento, no está claro cuándo podremos seguir avanzando. Nos gustaría tener el apoyo para transmitir esta tecnología a otros países".
Las investigaciones también acarrearon varias sorpresas, según los científicos. Una de ellas fue que el proceso de edición se producía de una manera inusual: los embriones inyectados con CRISPR parecían utilizar el gen materno sano para guiar el proceso de corrección de la mutación, mientras que ignoraban una plantilla de ADN proporcionada por los científicos.
Mitalipov cree que este fenómeno podría motivar que la técnica cambie de nombre. En vez de edición genética, tendría más sentido denominarla como una forma asistida de reparación natural del ADN. Relajando el debate, este razonamiento significaría que los niños nacidos de tales embriones podrían no ser, en sentido estricto, considerados como genéticamente modificados.


