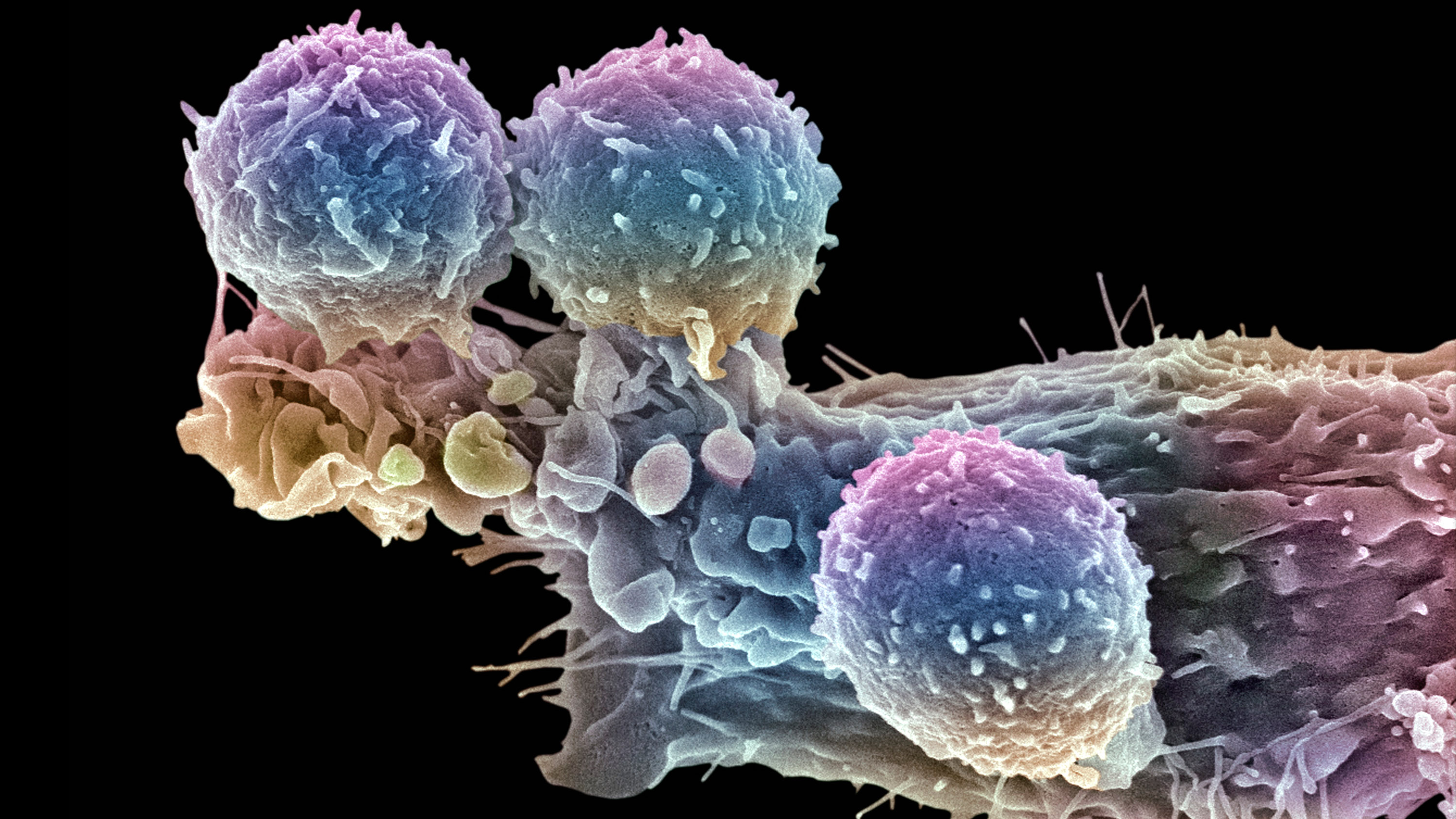
Las células CAR-T podrían revolucionar el tratamiento de una gran variedad de enfermedades, si tan sólo consiguiéramos abaratarlas.
Este artículo apareció por primera vez en The Checkup, el boletín semanal de biotecnología del MIT Technology Review. Para recibirlo en su bandeja de entrada todos los jueves y leer artículos como este primero, regístrese aquí .
Las terapias CAR-T, creadas mediante la ingeniería de las propias células del paciente para combatir el cáncer, suelen reservarse para personas que han agotado otras opciones de tratamiento. Pero la semana pasada, la FDA aprobó Carvykti, un producto CAR-T para el mieloma múltiple, como terapia de segunda línea. Esto significa que las personas pueden recibir Carvykti después de su primera recaída.
Si bien esto significa que algunos pacientes con mieloma múltiple en los EE.UU. tendrán ahora un acceso más temprano a CAR-T, la gran mayoría de los pacientes en todo el mundo todavía no recibirán CAR-T en absoluto. Estas terapias son caras: medio millón de dólares en algunos casos. ¿Pero tienen por qué serlo?
Echemos un vistazo a los esfuerzos por abaratar y hacer más accesibles las CAR-T.
No es difícil entender por qué las CAR-T tienen un precio tan elevado. La creación de estas terapias es un proceso de varios pasos. En primer lugar, los médicos extraen células T del paciente. A continuación, esas células se manipulan fuera del organismo mediante un vector vírico que inserta un gen artificial que codifica un receptor de antígeno quimérico o CAR. Este receptor permite a las células identificar las células cancerosas y marcarlas para su destrucción. A continuación, las células deben cultivarse en el laboratorio hasta que se cuenten por millones. Mientras tanto, el paciente debe someterse a quimioterapia para destruir los linfocitos T restantes y dejar espacio para las células CAR-T. A continuación, las células modificadas se reintroducen en el organismo del paciente, donde se convierten en fármacos vivos que combaten el cáncer. Es un proceso laborioso y de alta tecnología.
En Estados Unidos, las CAR-T generan mucho dinero. El precio de las terapias oscila entre 300.000 y 600.000 dólares, pero algunas estimaciones sitúan el coste real -que cubre el tiempo de hospitalización, los cuidados necesarios para tratar las reacciones adversas, etc.- en más de un millón de dólares en algunos casos.
Una forma de reducir costes es producir la terapia en países donde el desarrollo y la fabricación de fármacos son mucho más baratos. En marzo, la India aprobó su primera terapia CAR-T nacional, NexCAR19. La produce una pequeña biotecnología llamada ImmunoACT, con sede en Bombay. La terapia CAR-T india cuesta aproximadamente una décima parte de lo que cuestan los productos estadounidenses: entre 30.000 y 50.000 dólares. “El coste de producción de las células CAR-T, incluso en lugares como Estados Unidos, nos hace reflexionar”, afirma Terry Fry, hematólogo pediátrico del Anschutz Medical Campus de la Universidad de Colorado.
Ese menor coste se debe a diversos factores. La mano de obra es más barata en la India, donde se desarrolló y probó el fármaco y donde ahora se fabrica. La empresa también ha ahorrado dinero fabricando sus propios vectores virales, una de las partidas más caras del proceso de fabricación.
Otra forma de reducir costes es producir las terapias en los centros médicos donde se administran. Aunque los centros oncológicos se encargan de recoger las células T de sus pacientes, no suelen producir las terapias CAR-T ellos mismos. En su lugar, envían las células a las empresas farmacéuticas, que cuentan con instalaciones especializadas para la ingeniería y el cultivo de las células. A continuación, la empresa devuelve la terapia. Pero la producción propia de estas terapias -un modelo denominado fabricación en el punto de atención- podría ahorrar dinero y reducir los tiempos de espera. Un hospital de Barcelona fabricó y probó su propia terapia CAR-T y ahora la suministra a los pacientes por 97.000 dólares, una fracción de lo que cuestan los medicamentos de marca.
En Brasil, la Fundación Oswaldo Cruz, fabricante de vacunas y el mayor instituto de investigación biomédica de América Latina, se asoció recientemente con una organización sin ánimo de lucro estadounidense llamada Caring Cross para ayudar a desarrollar capacidades locales de fabricación de CAR-T. Caring Cross ha desarrollado un proceso de fabricación en el punto de atención capaz de generar terapias CAR-T por un coste aún menor: unos 20.000 dólares en materiales y 10.000 dólares en mano de obra e instalaciones.
Es un modelo atractivo. La demanda de CAR-T suele superar a la oferta, lo que provoca largos tiempos de espera. “Hay una tensión creciente en torno al acceso limitado que estamos viendo para las terapias celulares y genéticas que salen de la biotecnología”, dijo a Stat la oncóloga pediátrica de Stanford (California, EE UU) Crystal Mackall. “Es increíblemente tentador decir: «Bueno, ¿por qué no me dejáis fabricarlo para mis pacientes?»”.
Incluso estos tratamientos cuestan decenas de miles de dólares, en parte porque los productos CAR-T aprobados son terapias a medida, cada una producida para un paciente concreto. Pero muchas empresas también trabajan en terapias CAR-T listas para usar. En algunos casos, esto significa diseñar células T a partir de donantes sanos. Algunas de estas terapias ya están en fase de ensayo clínico.
En otros casos, las empresas trabajan en el diseño de células dentro del organismo. Este proceso debería simplificar y abaratar enormemente la administración de CAR-T. Con las terapias CAR-T convencionales, los pacientes tienen que someterse a quimioterapia para destruir las células T existentes. Pero con las CAR-T in vivo, este paso no es necesario. Y como estas terapias no requieren ninguna manipulación celular fuera del cuerpo del paciente, “se podrían administrar en una clínica ambulatoria”, afirma Priya Karmali, directora de tecnología de Capstan Therapeutics, que está desarrollando terapias CAR-T in vivo. “No necesitarías centros especializados”.
Algunas estrategias in vivo, al igual que las ex vivo, se basan en vectores virales. La plataforma de Umoja Biopharma utiliza un vector vírico, pero también emplea una segunda tecnología para inducir a las células modificadas a sobrevivir y expandirse en presencia del fármaco rapamicina. El otoño pasado, la empresa comunicó que había logrado generar células CAR-T in vivo en primates no humanos.
En Capstan Therapeutics, los investigadores están adoptando un enfoque diferente, utilizando nanopartículas lipídicas para transportar el ARNm a las células T. Cuando un vector viral introduce el gen CAR en el ADN de una célula, el cambio es permanente. Cuando un vector vírico introduce el gen CAR en el ADN de una célula, el cambio es permanente. Pero con el ARNm, el CAR sólo actúa durante un tiempo limitado. “Una vez terminada la guerra, no queremos que los soldados sigan merodeando por ahí para siempre”, afirma Karmali.
Y con CAR-T, hay muchos campos de batalla potenciales que conquistar. Las terapias CAR-T ya son prometedoras más allá de los cánceres sanguíneos. A principios de este año, los investigadores comunicaron resultados sorprendentes en 15 pacientes con lupus y otras enfermedades autoinmunes. Las CAR-T también se están probando como tratamiento de tumores sólidos, cardiopatías, envejecimiento e infección por VIH, entre otras. A medida que aumente el número de personas susceptibles de recibir terapias CAR-T, también lo hará la presión para reducir su coste.
Ahora lea el resto de The Checkup.
Lea más del archivo de MIT Technology Review
Los científicos finalmente están avanzando en la introducción de CAR-T en tumores sólidos. El otoño pasado escribí sobre las barreras y el progreso .
En los primeros días de CAR-T, Emily Mullin informó sobre muertes de pacientes que ponía en duda la seguridad del tratamiento.
Viaja en el tiempo para revivir la emoción por la aprobación de la primera terapia CAR-T con esta historia de Emily Mullin.
De toda la web
La Corte Suprema de Arizona dictaminó que una ley de 1864 que prohíbe casi todos los abortos puede aplicarse después de un período de gracia de 14 días. ( NBC )
La escasez de medicamentos es peor de lo que ha sido en más de dos décadas. Los analgésicos, los medicamentos de quimioterapia y los medicamentos para el TDAH son escasos. Este es el por qué. ( Estadística )
Inglaterra se convirtió en el quinto país europeo en comenzar a limitar el acceso de los niños a tratamientos de género como bloqueadores de la pubertad y terapia hormonal. Los defensores de las restricciones dicen que hay poca evidencia de que estas terapias ayuden a los jóvenes con disforia de género. ( NYT )
La semana pasada escribí sobre un brote de gripe aviar en vacas. Un nuevo estudio encuentra que las aves de la ciudad de Nueva York también son portadoras del virus. Los investigadores encontraron H5N1 en gansos del Bronx, un pollo en Manhattan, un halcón de cola roja en Queens y un ganso y un halcón peregrino en Brooklyn. ( NYT )


