El experimento para tratar el párkinson es una primera prueba decisiva que muestra el potencial de las células madre para combatir enfermedades graves
En una importante prueba para la medicina de células madre, una empresa de biotecnología afirma que los implantes de neuronas fabricadas en laboratorio e introducidas en los cerebros de 12 personas con enfermedad de párkinson parecen seguros y pueden haber reducido los síntomas para algunos pacientes.
Las células añadidas deben producir el neurotransmisor dopamina, cuya escasez es lo que produce los devastadores síntomas del Parkinson, incluidos los problemas de movimiento.
"El objetivo es que formen sinapsis y hablen con otras células como si fueran de la misma persona", afirma Claire Henchcliffe, neuróloga de la Universidad de California en Irvine y una de las responsables del estudio. "Lo interesante es que se pueden administrar estas células y pueden hablar con el huésped".
El estudio es, hasta la fecha, una de las pruebas más grandes y costosas de la tecnología de células madre embrionarias. Un método tan controvertido como publicitado que utiliza células madre extraídas de embriones de fecundación in vitro para producir tejidos y partes del cuerpo de sustitución.
El ensayo a pequeña escala tenía el objetivo principal de demostrar la seguridad del método y fue patrocinado por BlueRock Therapeutics, una filial del gigante farmacéutico Bayer. Las neuronas de sustitución fueron fabricadas con potentes células madre obtenidas originalmente de un embrión humano que había sido creado mediante un procedimiento de fecundación in vitro.
Según los datos presentados por Henchliffe y sus compañeros el 28 de agosto en el Congreso Internacional para la Enfermedad de Párkinson y Trastornos del Movimiento (MDS, por sus siglas en inglés) en Copenhague, también hay indicios de que las células añadidas habían sobrevivido y reducían los síntomas de los pacientes un año después del tratamiento.
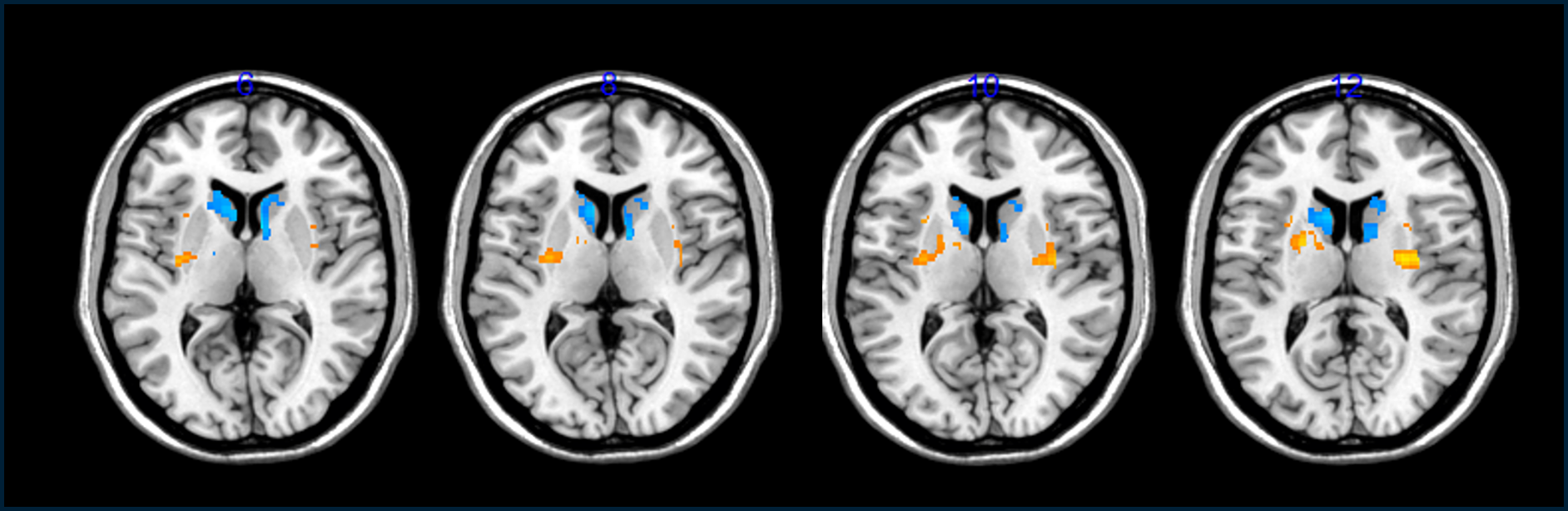
Estas pistas de que los trasplantes ayudaron procedían de escáneres cerebrales que mostraban un aumento de las células dopaminérgicas en el cerebro de los pacientes. Así como una disminución del tiempo de desconexión, o el número de horas al día que los voluntarios se sentían incapacitados por sus síntomas.
Sin embargo, expertos externos se mostraron cautelosos al interpretar los resultados, ya que parecían mostrar efectos inconsistentes, algunos de estos podrían deberse al efecto placebo y no al tratamiento.
"Es alentador que el ensayo no haya dado lugar a ningún problema de seguridad y haya algunos beneficios", asegura Roger Barker, que estudia la enfermedad de párkinson en la Universidad de Cambridge (Reino Unido). Pero Barker calificó como "un poco decepcionantes" las pruebas de que las células trasplantadas habían sobrevivido.
Como los investigadores no pueden ver las células de manera directa una vez que están en la cabeza de una persona, en su lugar, rastrean su presencia al administrar a las personas un precursor radiactivo de la dopamina. Después, observan su captación en el cerebro en un escáner PET. Para Barker, estos resultados no fueron tan contundentes y afirma que "aún es demasiado pronto para saber" si las células trasplantadas se afianzaron y repararon el cerebro de los pacientes.
Preguntas legales
Las células madre embrionarias se aislaron por primera vez en 1998 en la Universidad de Wisconsin, a partir de embriones obtenidos en clínicas de fertilidad. Son útiles para los científicos porque pueden cultivarse en el laboratorio y, en teoría, ser inducidas a formar cualquiera de los casi 200 tipos celulares del cuerpo humano. Esto ha propiciado intentos de restaurar la visión, curar la diabetes y revertir lesiones de la médula espinal.
Sin embargo, aún no existe ningún tratamiento médico basado en células madre embrionarias, a pesar de los miles de millones de dólares invertidos en investigación por gobiernos y empresas en estos últimos 25 años. El estudio de BlueRock es todavía uno de los principales intentos de cambiar esta situación.
Además, las células madre siguen planteando cuestiones delicadas en Alemania, donde Bayer tiene su sede. Según la Ley de Protección de Embriones alemana, una de las más restrictivas del mundo, obtener células de un embrión todavía es un delito punible con penas de cárcel.
En determinadas circunstancias, sí es legal utilizar suministros de células existentes en el extranjero, siempre que se hayan creado antes de 2007. Seth Ettenberg, presidente y CEO de BlueRock, afirma que la empresa fabrica neuronas en EE UU, y para ello emplea células madre embrionarias procedentes de los suministros originales de Wisconsin, que siguen siendo utilizados.
"Todas las operaciones de BlueRock respetan los elevados estándares éticos y legales de la Ley de Protección de Embriones alemana, dado que BlueRock no lleva a cabo ninguna actividad con embriones humanos", respondió Nuria Aiguabella Font, portavoz de Bayer, en un correo electrónico.
Una larga historia
La idea de sustituir las células productoras de dopamina para tratar el párkinson se remonta a la década de 1980, cuando los médicos lo intentaron con neuronas fetales recogidas tras los abortos. Aquellos estudios resultaron equívocos. Aunque algunas personas pudieron beneficiarse, los experimentos generaron titulares alarmantes después de que otros pacientes desarrollaran efectos secundarios "de pesadilla", como retorcimientos y sacudidas incontrolados.
Utilizar células cerebrales de fetos no solo era éticamente dudoso para algunos. Los investigadores también estaban convencidos de que ese tejido era tan variable y difícil de obtener que no podía convertirse en un tratamiento estandarizado. "Hay antecedentes de intentos de trasplante de células o fragmentos de tejido en cerebros", explica Henchcliffe. "Ninguno llegó a buen puerto, y creo que en el pasado hubo una falta de comprensión del mecanismo de acción, y una falta de suficientes células de calidad controlada".
Sin embargo, había pruebas de que las células trasplantadas podían vivir. Los exámenes post-mortem de algunos pacientes tratados con células fetales mostraron que los trasplantes seguían presentes muchos años después. "Hay un montón de gente implicada en esos trasplantes de células fetales. Siempre quisieron averiguar ‘si lo hacías bien, ¿funcionaría?’", cuenta Jeanne Loring, cofundadora de Aspen Neuroscience, una empresa de células madre que planea lanzar sus propias pruebas para tratar la enfermedad de párkinson.
El descubrimiento de las células madre embrionarias hizo posible una prueba más controlada. Estas células pueden multiplicarse y convertirse en miles de millones en células productoras de dopamina.
Los trabajos iniciales para fabricar dichas células dopaminérgicas, así como las pruebas en animales, corrieron a cargo de Lorenz Studer en la Universidad de Columbia (Nueva York). En 2016, Studer se convirtió en fundador científico de BlueRock, que se formó inicialmente como una empresa conjunta entre Bayer y Versant Ventures, una sociedad de inversión
"Es una de las primeras veces que hemos tenido un producto tan bien entendido y uniforme con el que trabajar", reconoce Henchcliffe, que participó en los primeros esfuerzos de BlueRock. En 2019, Bayer tomó el control total de la empresa de células madre en un acuerdo que la valoró en alrededor de mil millones de dólares.
Trastorno del movimiento
En la enfermedad de párkinson, las células que producen dopamina mueren, y esto provoca una escasez de esta sustancia química cerebral. Esto puede provocar temblores, rigidez en las extremidades y una disminución general del movimiento denominada bradicinesia. La enfermedad suele ser lenta, y el fármaco levodopa puede controlar los síntomas durante años. El estimulador cerebral profundo, un tipo de implante cerebral, también puede reducir los síntomas. Sin embargo, la enfermedad es progresiva y, con el tiempo, la levodopa no puede controlar tan bien los síntomas.
 BLUE ROCK THERAPEUTICS
BLUE ROCK THERAPEUTICS
En 2023, el actor Michael J. Fox confesó a la CNN que se retiró definitivamente de la actuación debido a que ya no podía recordar sus diálogos, aunque eso fue 30 años después de su diagnóstico. "No voy a mentir. Cada vez es más difícil", contó Fox a la cadena. "Cada día es más duro".
La promesa de una terapia celular es que los médicos no se limitarían a poner parches a los síntomas, sino que podrían sustituir las redes cerebrales rotas al añadir nuevas neuronas.
"El potencial de la medicina regenerativa no solo es retrasar la enfermedad, sino reconstruir la funcionalidad del cerebro", explica Ettenberg, CEO de BlueRock. "Esperamos que algún día la gente no piense en sí misma como paciente de párkinson".
Ettenberg afirma que BlueRock tiene previsto iniciar un estudio más amplio, con más pacientes, el año que viene, y determinar si el tratamiento funciona y con qué eficacia.


