Todas ellas indican que la FDA parece no estar siendo demasiado estricta en sus regulaciones, aunque las clínicas se defienden al afirmar que no hay pruebas de que sus tratamientos no sean seguros
Al menos hay 351 empresas por todo Estados Unidos que ofrecen intervenciones con céulas madres no demostradas que afirman servir para tratar casi cualquier cosa, desde artritis hasta la enfermedad de Alzheimer, según un trabajo publicado el pasado jueves por la revista Cell Stem Cell. El hallazgo arroja luz sobre una emergente era de tratamientos médicos que han recibido poca atención por parte de la Agencia de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inlgés).
"Con estos datos resulta dificil creer que la FDA esté haciendo un buen trabajo con la regulación del mercado", afirma el experto en bioética de la Universidad de Minnesota (EEUU) Leigh Turner, que realizó el estudio junto con el investigador de células madre de la Universidad de California en Davis (EEUU) Paul Knoepler.
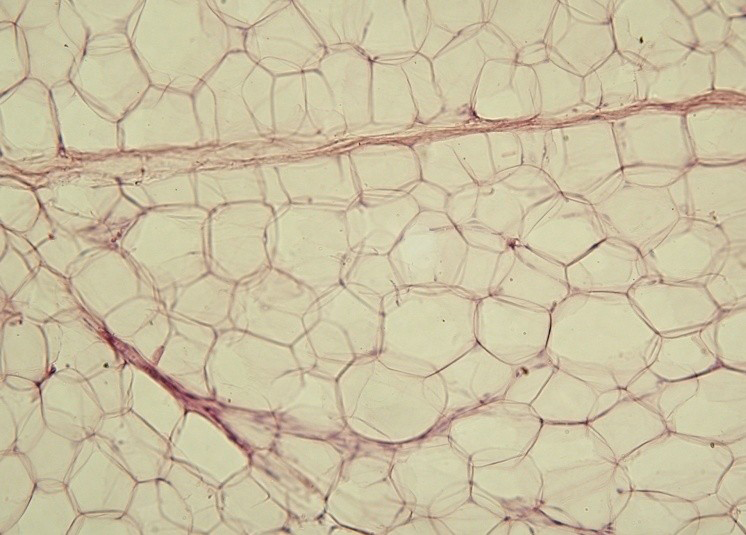
 Foto: Un cubrobjetos de microscopio preparado con una muestra de tejido adiposo blanco. Las células madre de adipocitos de los pacientes son obtenidas mediante una liposucción y a menudo son simplemente reinyectadas al riego sanguíneo del mismo paciente con la esperanza de que lleguen a su destino objetivo. Crédito: Departamento de Histología de la Facultad de Medicina de la Universidad Jagelónica (Polonia).
Foto: Un cubrobjetos de microscopio preparado con una muestra de tejido adiposo blanco. Las células madre de adipocitos de los pacientes son obtenidas mediante una liposucción y a menudo son simplemente reinyectadas al riego sanguíneo del mismo paciente con la esperanza de que lleguen a su destino objetivo. Crédito: Departamento de Histología de la Facultad de Medicina de la Universidad Jagelónica (Polonia).
Las preocupaciones sobre las terapias de células madre sin regular no son nuevas, pero anteriormente se creía que el tema se limitaba a pacientes que viajaban al extranjero para recibir tratamientos no disponibles o expresamente prohibidos en territorio nacional. Esos tratamientos renegados pueden ser ineficaces y peligrosos. La semana pasada, la revista New England Journal of Medicine describió un incidente en el que unos cirujanos descubrieron una masa pegajosa de células ajenas en la médula de un paciente tras haber recibido inyecciones de células madre fetales en varios países distintos.
El nuevo estudio de Knoepfler y Turner demuestra que 570 clínicas por todo el país están ofreciendo tratamientos similares, con tal vez decenas de miles de pacientes al año. "Si sólo existiesen una o dos operaciones clandestinas no sería un problema, pero esto parece un enorme fallo de las regulaciones", afirma Turner.
Las regulaciones de la FDA están diseñadas para abordar qué tipos de terapias basadas en células requieren la aprobación de la agencia y cuáles no. Una de las mayores restricciones es aplicada a las llamadas terapias de célula madre no homólogas: los médicos no deben extraer células de un tejido para después colocarlas en otro órgano no relacionado. Extraer células grasas del abdomen de un paciente para después inyectárselas al cerebro para tratar la enfermedad de Alzheimer estaría en esa categoría con casi total seguridad.
Pero es exactamente lo que hacen algunas de estas clínicas. Sus terapias a menudo hacen uso de células madre de adipocitos, tal vez porque el procedimiento resulta fácil. Los médicos emplean la liposucción para obtener células grasas de un paciente. Entonces las licuan junto con enzimas, separan las células en una centrifugadora y se las vuelven a inyectar al paciente. Los detalles varían, pero las clínicas a menudo alegan que el proceso cumple con las regulaciones de la FDA.
 Foto: Un mapa muestra dónde están radicadas las clínicas estudiadas. Las estrellas azules indican ciudades donde este negocio es especialmente prominente. Crédito: Leigh Turner y Paul Knoepfler.
Foto: Un mapa muestra dónde están radicadas las clínicas estudiadas. Las estrellas azules indican ciudades donde este negocio es especialmente prominente. Crédito: Leigh Turner y Paul Knoepfler.
La FDA puede que no se muestre de acuerdo. El año pasado lanzó un borrador de directrices, que aún no es de aplicación legal, que afirma que este proceso altera demasiado las células y por tanto debería ser sujeto a la aprobación de la FDA al igual que los fármacos.
El investigador de políticas públicas en el Instituto Tecnológico de Georgia (EEUU) Aaron Levine dice que el trabajo de Knoepfler y Turner "debería servir como una llamada de atención", o al menos "señalar a la FDA la magnitud del problema".
Pero, mientras que muchos investigadores afirman que la FDA debería regular estos procedimientos, los médicos que trabajan en estas clínicas a menudo lo consideran innecesario. "Sería un enorme error", afirma el director de la clínica Manhattan Spine and Sports Medicine, Drew DeMann. "No creo que sea un fármaco, sólo consiste en emplear tejido de nuestro propio cuerpo en distintos lugares", afirma. En su opinión, las células madre procedentes del túetano y los tejidos grasos son una herramienta "indispensable" para tratar lesiones deportivas, trastornos ortopédicos y el dolor. "No existe ninguna indicación de que no sea seguro", asegura.
Knoepfler y Turner encontraron que la ortopedia era el campo más frecuente en las clínicas de células madre, con más de 300 negocios que ofrecen estas terapias. DeMann reconoce que la eficacia de estos tratamientos se merece un estudio más detallado, pero también afirma: "No creo que los profesionales médicosdeban esperar hasta que exista un grado abrumador de pruebas".
Algunos profesionales médicos tienen sentimientos contradictorios sobre las regulaciones de célula madre. "Necesitamos hacer algo respecto a la regulación de estas clínicas", asegura el fundador de Chimera Labs, una clínia de células madre radicada en Miami (EEUU), Duncan Ross. Le preocupa que la gestión indebida por parte de técnicos de laboratorio poco experimentados pueda contaminar las células, un problema que afirma haber solucionado en su propio laboratorio.
Actualmente, intenta tratar la enfermedad pulmonar obstructiva crónica (EPOC) con inyecciones de células grasas en riego sanguíneo de los pacientes. Esto parece contradecir las reglas de la FDA en contra de extraer un tipo de célula y colocarla en otro órgano distinto. "Es verdad, es no homólogo, ¿y qué? No ha dañado a nadie hasta ahora", dice Ross..
Pero a Turner le preocupan las clínias que promocionan terapias para enfermedades como el Alzhemier, como 27 clínicas identificadas por el estudio. "Si alguien padece una enfermedad terminal y empieza a buscar un rayo de esperanza en internet, encontrará una gran proliferación de negocios que parecen ser profesionales y atractivos y parecen estar vinculados con investigadores y estudios preclínicos fidedignos", explica. Eso puede dar paso a un peligroso atractivo que carece de historial demostrable de eficacia, e incluso de seguridad.
A pesar del vasto número de clínicas de células madre activas, la FDA sólo ha emitido un puñado de cartas advirtiéndoles de que sus procedimientos han de someterse a la aprobación de la FDA bajo la clasificación de fármacos biológicos. Knoepfler dice que eso genera "una desconexión entre la magnitud de la industria de las células madre y las medidas para regularla". Las investigaciones de células madre han avanzado mucho durante los últimos 10 años, pero a Knoepfler le gustaría que se prestara menos atención a las terapias controvertidas y no demostradas que reciben los deportistas y las celebridades. "Realmente me siento muy optimista sobre el campo en general, y observaremos la finalización de un número importante de ensayos clínicos durante la próxima década. Simplemente no hemos llegado lo suficientemente lejos", concluye.


