Este julio, hace cuarenta y ocho años, Louise Joy Brown se convirtió en la primera persona del mundo nacida con la ayuda de la fecundación in vitro. Millones más de bebés FIV han llegado al mundo desde entonces. Y eso es en parte gracias a los avances tecnológicos que han hecho que la FIV sea más segura y eficaz.
Pero todavía no es perfecto. El proceso puede ser lento, doloroso y costoso —y eso es para las personas afortunadas que logran acceder a él en primer lugar. Y, según al menos un indicador, las tasas de éxito de la FIV han estado disminuyendo en los últimos años.
La reproducción es compleja, y hay mucho que los embriólogos y ginecólogos todavía no saben y no pueden controlar. No saben por qué muchos embriones de aspecto saludable no se «implantan» en el útero, por ejemplo. No siempre tienen una explicación de por qué sus pacientes no pueden quedarse embarazadas. Y no siempre pueden explicar las grandes diferencias en las tasas de éxito de la FIV entre individuos y entre clínicas de fertilidad.
Los científicos están trabajando en todas esas preguntas y más. Están lidiando con complejas cuestiones éticas sobre cómo se utilizarán las nuevas herramientas genéticas para analizar o incluso alterar embriones. Mientras tanto, las tecnologías diseñadas para estandarizar el tratamiento, eliminar el error humano, mejorar las tasas de éxito y hacer más accesible la FIV ya están empezando a dar paso a una nueva era para la reproducción asistida, una asistida por IA y robots.
1. Facilitar la implantación de los embriones
Algunas de esas tecnologías se desarrollan en la Fundación Carlos Simón, en Valencia, España. Cuando visité en marzo, los investigadores me hicieron un recorrido por los laboratorios y me mostraron un dispositivo que se había utilizado para mantener un útero humano vivo fuera del cuerpo por primera vez.
Aunque algunos miembros del equipo sueñan con construir úteros artificiales que algún día podrían llevar un feto a término, primero quieren usar estos dispositivos para aprender más sobre la implantación —el momento en que un óvulo fecundado hace contacto con el revestimiento del útero, se introduce en su interior y, esencialmente, "eclosiona"—, desencadenando el inicio de un embarazo.
A pesar de décadas de avances en la FIV, ese proceso aún se entiende poco. Incluso los embriones de aspecto saludable no se implantan más del 40% al 60% de las veces.
En las técnicas de FIV utilizadas hoy en día, las clínicas pueden crear embriones en fase temprana y esperar hasta que el útero se considere más receptivo, pero una vez que insertan el embrión en el útero, este queda a su suerte. Xavier Santamaría, científico clínico sénior de la Fundación Carlos Simón, y sus colegas están ensayando un enfoque diferente. Han desarrollado un dispositivo que, con solo pulsar un botón, inyecta el embrión en el revestimiento uterino.
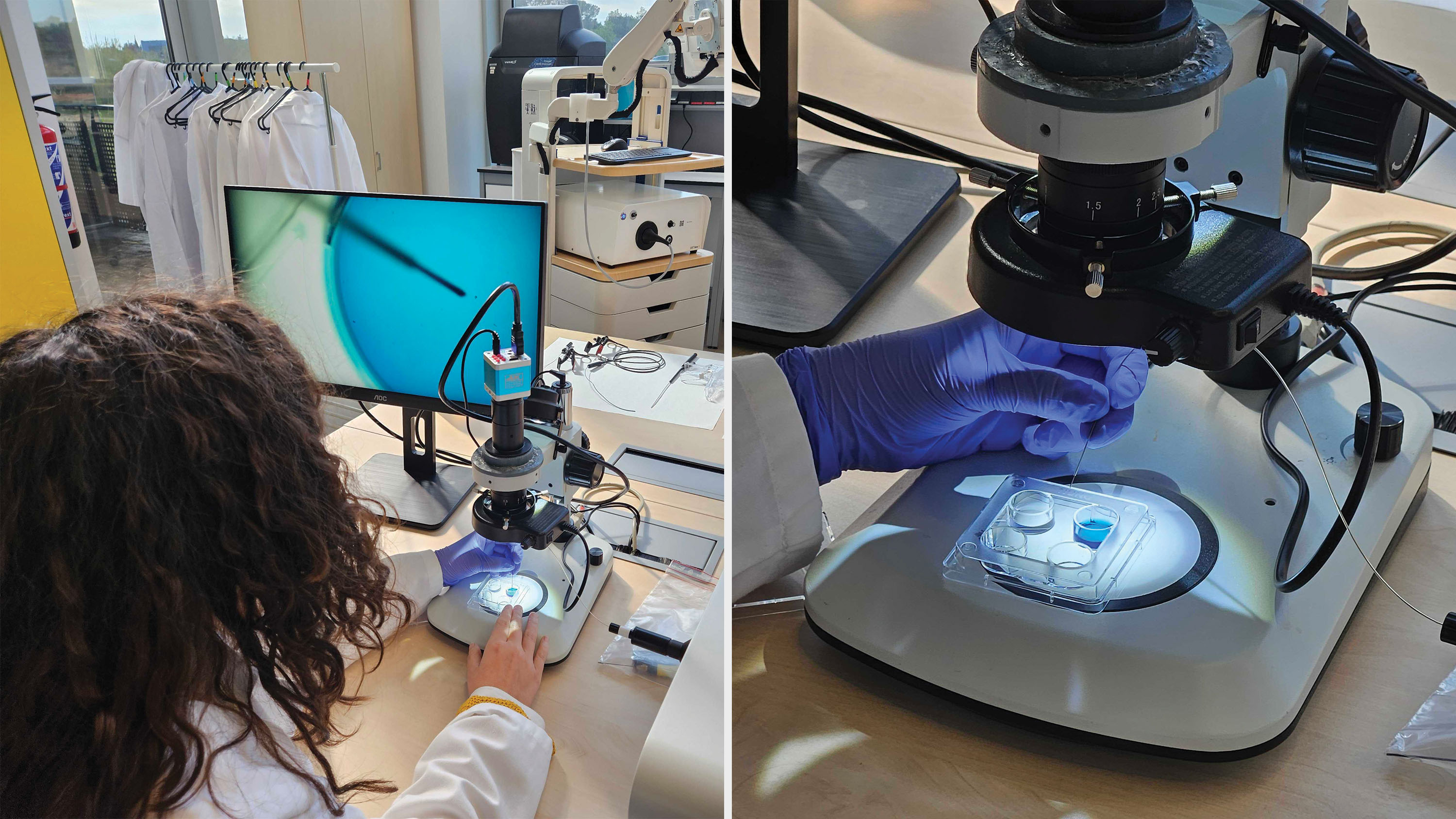
En una demostración que presencié con un prototipo, Santamaría cogió su espéculo y se volvió hacia la abertura vaginal de su “paciente”, que en este caso era solo un modelo de la realidad —un torso inferior de plástico con labios, una vagina, un útero y ovarios, dos tocones cortos que representaban lo que normalmente serían un par de pie as sujetas en estribos.
Se inclinó y miró dentro. «Embrión», dijo. Su colega María Pardo, una embrióloga, le pasó una aguja fina que contenía un embrión de ratón que había recogido recientemente de una placa de Petri.
El dispositivo de Santamaría permite que la aguja que contiene el embrión se conecte a un tubo de administración. Este tubo también tiene una cámara, una luz y un sensor que permite al médico saber cuándo la aguja alcanza el revestimiento uterino. Una vez que ha sido introducido en el útero, el ginecólogo puede ver el interior del órgano y dirigir el tubo al revestimiento.

“Cuando todo está listo, solo tienes que pulsar el botón”, dijo Santamaría mientras lo activaba con un pedal, permitiendo que el embrión fuera inyectado. “Ahí va”.
El equipo acaba de comenzar un ensayo del dispositivo; hasta ahora, menos de 10 mujeres se han sometido al procedimiento, y ninguna de ellas ha quedado embarazada. Pero el director de la fundación, Carlos Simón, se muestra optimista, señalando que los inventores de la FIV tuvieron que realizar más de 160 ciclos antes del nacimiento de Louise Brown (entre 1969 y 1978, ese equipo realizó 457 ciclos en 250 personas, resultando en solo dos nacimientos vivos). “El ensayo está en curso”, afirma.
2. La selección de los «mejores» óvulos, espermatozoides y embriones
Uno de los retos constantes de la fecundación in vitro (FIV) ha sido la selección. Supongamos que se logran recolectar 10 óvulos de uno de los miembros de la pareja y una muestra de semen de buen aspecto del otro. ¿Cómo elegir qué células utilizar? La misma cuestión surge una vez que los embriones resultantes han sido cultivados en una placa durante unos días: ¿cuáles se deben transferir al útero?
Tradicionalmente, estas valoraciones se han realizado a simple vista. Los embriólogos eligen literalmente los que mejor aspecto tienen en cuanto a su forma o, en el caso de los espermatozoides, por su movimiento. Pero los científicos han estado trabajando en alte ativas. Y en la última década, aproximadamente, muchos han recurrido a las pruebas genéticas para indicar qué embriones tienen las mejores probabilidades de dar lugar a un bebé sano.
La prueba más utilizada se denomina PGT-A, siglas que corresponden a 'diagnóstico genético preimplantacional de aneuploidías'. La aneuploidía, en esencia, se refiere a la presencia de un número 'incorrecto' de cromosomas, y se considera que los embriones con tales características tienen más probabilidades de sufrir una pérdida gestacional por aborto espontáneo o de convertirse, potencialmente, en bebés con afecciones genéticas.
Una vez que los embriólogos han creado embriones en el laboratorio, pueden extraer unas pocas células y analizarlas en busca de aneuploidías. Estas pruebas son especialmente beneficiosas para mujeres mayores de 38 años, afirma Alan Penzias, endocrinólogo reproductivo en Boston IVF. «Se empieza a observar una mejora: más bebés y menos abortos espontáneos», comenta. Las pruebas pueden acortar el tiempo hasta el embarazo.
Este tipo de pruebas genéticas es posible gracias a múltiples avances tecnológicos —no solo en genómica, sino también en la capacidad de mantener embriones vivos en una placa durante cinco o seis días y en la técnica de congelar embriones mientras las células se someten a pruebas, para luego descongelarlos una vez que se obtienen los resultados. Y se ha vuelto enormemente popular —algunas clínicas realizan pruebas PGT-A en todos sus embriones.
Pero el PGT-A no ofrecerá una lectura perfecta de la genética de un futuro bebé, afirma Sonia Gayete-Lafuente, endocrinóloga reproductiva en el Centro de Reproducción Humana de Nueva York. Y algunas de las anomalías podrían corregirse por sí mismas con el tiempo. Gayete-Lafuente y sus colegas han transferido algunos de esos embriones «anormales» a los úteros de las pacientes y los han visto desarrollarse hasta convertirse en niños perfectamente sanos, añade.
Otras formas de PGT son aún más controvertidas. Las pruebas PGT-P están diseñadas para predecir las posibilidades de un embrión de desarrollar rasgos complejos que dependen de múltiples genes, incluyendo trasto os médicos, pero también características físicas como la altura o factores cognitivos como el coeficiente intelectual. Estas pruebas son nuevas y son ilegales en algunos países, incluyendo el Reino Unido. Pero están ganando terreno en EE. UU. Nucleus Genomics —una empresa que invita a los clientes a “tener [su] mejor bebé”— promete predecir rasgos que abarcan desde el color de ojos y la inteligencia hasta la zurdera y el riesgo de Alzheimer.
Cuando pregunté a los especialistas en FIV cómo responderían si un paciente solicitara este servicio, la mayoría esquivó la pregunta y me dijo que no hay pruebas suficientes de que ninguna de estas pruebas funcione realmente. También advirtieron que seleccionar un rasgo concreto podría introducir nuevos riesgos de forma inadvertida. Ninguno parecía especialmente partidario de la idea de utilizar las pruebas genéticas para otra cosa que no fuera prevenir enfermedades graves.
3. Agilizando los procesos con IA
Algunos se mostraron más entusiasmados con el potencial de la IA. Al fin y al cabo, las herramientas de IA son generalmente buenas para reconocer patrones. Muchos investigadores han intentado entrenar herramientas para identificar espermatozoides, óvulos y embriones sanos.
Y han cosechado cierto éxito. Un equipo del Centro Médico de la Universidad de Columbia en Nueva York ha desarrollado un dispositivo que utiliza IA para examinar muestras de semen de hombres que tienen un número ínfimo de espermatozoides sanos. Un embriólogo podría encontrar grandes dificultades para hallar un solo espermatozoide sano en una muestra así. Pero el sistema de Seguimiento y Recuperación de Espermatozoides (STAR) puede analizar más de un millón de imágenes de microscopio en una hora. Ya se ha utilizado para crear embriones sanos. El equipo responsable del trabajo anunció el primer embarazo resultante del tratamiento en noviembre del año pasado.
Otros equipos están utilizando herramientas de IA para impulsar la Fecundación In Vitro (FIV) de formas más drásticas. Hace aproximadamente una década, un endocrinólogo reproductivo llamado Alejandro Chávez-Badiola comenzó a desarrollar una herramienta de IA entrenada para clasificar embriones, otra para clasificar óvulos y otra para seleccionar espermatozoides. Recuerda haber sido impactado por la revelación de que estas herramientas eran «los cerebros que tienen el potencial de impulsar robots en el futuro», afirma.
4. Utilización de robots para estandarizar la FIV
A principios de la década de 2020, Chávez-Badiola y sus colegas decidieron combinar tecnologías y desarrollar un sistema automatizado para la FIV. En teoría, un sistema robótico equipado con herramientas de IA podría llevar a cabo la mayoría de los pasos requeridos en el proceso de FIV: seleccionar los óvulos y el esperma, fecundar los óvulos para crear embriones, cultivar esos embriones en una placa y seleccionar el "mejor" para la transferencia. Dicho sistema podría "hacerlo todo de forma estandarizada" sin cansarse nunca, afirma.
Chávez-Badiola, quien ahora es fundador y director médico en Conceivable, empezó a construir prototipos motorizando equipos de FIV convencionales y conectándolos a ordenadores. Él y sus colegas comenzaron a probar su sistema con células animales antes de pasar finalmente a las humanas. "Pudimos demostrar que integrar robots para automatizar diferentes pasos en la FIV es factible", afirma.
Actualmente, el dispositivo se está utilizando para preparar espermatozoides y óvulos, y para crear embriones. Al menos 19 niños han nacido tras la FIV automatizada. Todavía es pronto, pero Chavez-Badiola espera que futuras iteraciones de la máquina puedan procesar cada una miles de ciclos de FIV al año, lo que podría hacer el procedimiento más asequible y accesible.
Muchos profesionales del sector están entusiasmados con el potencial de dispositivos automatizados como los de Conceivable. «Todo esto es tiempo ahorrado para los embriólogos», afirma Laura Rienzi, embrióloga clínica y directora científica de la red IVIRMA de centros de fertilidad en Italia. También espera que ayude a estandarizar los tratamientos de FIV. «La automatización [permitirá] que cada paciente reciba el mismo tratamiento en cualquier laboratorio del mundo», afirma.
5. Modificaciones controvertidas sobre la mesa
Sin embargo, hay un inconveniente: Todas estas tecnologías dependen de la disponibilidad de al menos algunos espermatozoides, óvulos y embriones sanos al principio. Los embriólogos y los pacientes de FIV tienen que trabajar con lo que tienen. Y a veces, lo que tienen no dará como resultado un bebé sano.
Por eso, algunos científicos están proponiendo una idea controvertida: utilizar tecnologías de edición genética como CRISPR para modificar el genoma de un embrión FIV antes de su implantación. El biofísico He Jiankui adoptó de forma infame este enfoque para crear embriones que resultaron en el nacimiento de tres niños a finales de la década de 2010. Fue ampliamente condenado por la comunidad científica y, finalmente, cumplió tres años en una prisión china.
Su expareja sentimental Cathy Tie, quien ahora dirige la startup Origin Genomics, está impulsando esta tecnología como una forma potencial de prevenir enfermedades graves en niños. En un evento reciente celebrado en el Hastings Center for Bioethics, Tie defendió el uso de la edición de embriones para prevenir enfermedades como la fibrosis quística, la enfermedad de Huntington y la anemia de células falciformes.
No será sencillo desde una perspectiva técnica, legal o ética. Las enfermedades que se sabe que son causadas por mutaciones monogénicas son buenas primeras candidatas, pero como señala Gayete-Lafuente del Centro para la Reproducción Humana, la mayoría de las enfermedades son mucho más complicadas que eso. «Ojalá pudiéramos comprender la base genética de cada enfermedad para poder prevenirla», afirma. Hasta ahora, no podemos. Además, la mayoría de las enfermedades pueden verse influidas por nuestras dietas, comportamientos y ento os, además de por nuestros genes.
Actualmente, nadie sabe si editar un embrión humano para eliminar el riesgo de una enfermedad podría aumentar el riesgo de algún otro trasto o en un futuro niño. Y algunos científicos temen que tales ediciones puedan ser una pendiente resbaladiza hacia la mejora genética o la eugenesia.
Rienzi espera que la tecnología pueda desarrollarse de forma segura, con supervisión regulatoria, y solo para una lista específica de enfermedades. "Tiene que estar dentro de un contexto legal", dice. "Pero para mí, es un sueño".
Mientras tanto, el sector parece abocado a seguir transformándose con el desarrollo de nuevas tecnologías que ya están haciendo posible el nacimiento de bebés sanos. Estén atentos.

