Cada vez hay más casos de pacientes que mejoran drásticamente gracias a fármacos diseñados para las mutaciones concretas de sus tumores. Pero nadie sabe por qué el enfoque solo funciona a veces

Crédito: Jonno Rattman.
A lo largo de los 30 años en los que luchó contra el cáncer de mama, Carmen Teixidor creía haber pasado por todos los tratamientos médicos disponibles contra la enfermedad. Había soportado múltiples rondas de radiación y múltiples ciclos de terapias hormonales. Probó la quimioterapia una vez, hace unos 25 años, pero disminuyó tanto su calidad de vida que ha intentado evitarla desde entonces. También se sometió a múltiples operaciones, y llegó desarrollar un miedo al momento en el que despertaba de la anestesia, ya que casi de forma inevitable iba a recibir nuevas malas noticias. Todo empezó durante el verano de 1985, cuando los médicos le descubrieron un gran tumor en su mama izquierda y se sintieron obligados a practicarle una mastectomía.
"Terror absoluto", recuerda, mirando el suelo de su piso en Nueva York (EEUU). Nunca hay un buen momento para diagnosticar un cáncer, pero para Teixidor la noticia llegó justo cuando su carrera como artista empezaba a despegar. Acababa de vender dos de sus esculturas a escala real al campus de la Universidad Rockefeller (EEUU), y hacía poco que había terminado un mural en el Hospital Harlem (EEUU). Esta delgada mujer que ahora está en la setentena, con su pelo gris recogido en una coleta juvenil, ha lidiado con una recaída tras otra, sometiéndose a herramientas médicas desde el bisturí hasta, más recientemente y tal vez de forma más improbable, la molécula.
Teixidor no prestó mucha atención a cuando sus médicos del Centro de Cáncer Sloan Kettering Memorial en Nueva York analizaron una pequeña muestra de su tumor y secuenciaron el ADN de sus células cancerosas en otoño de 2013. Era el mismo proceso que seguían varios centros de investigación del cáncer para buscar mutaciones que pudieran promover estos malignos desarrollos. Algunas de estas mutaciones son el objetivo de una nueva generación de fármacos diseñados específicamente para atacarlas.
Resultó que el tumor de Teixidor de hecho poseía varias mutaciones médicamente interesantes. Pero había un obstáculo: no existía ningún fármaco para a las suyas en particular. En otoño de 2013, esto no era algo preocupante, porque su cáncer, a pesar de muchas recaídas, parecía estar bajo control. Hasta que todo cambió.
 Foto: David Hyman es oncólogo del Centro de Cáncer Sloan Kettering Memorial. Crédito: Jonno Rattman.
Foto: David Hyman es oncólogo del Centro de Cáncer Sloan Kettering Memorial. Crédito: Jonno Rattman.
"Hace dos años hubo una recaída muy mala", recuerda la paciente. Sentía cómo los tumores se le sobresalían de la parte posterior del cráneo. Otro se arraigó en su mandíbula. Tenía tumores en el cuello, y las pruebas de imagen revelaron más tumores en sus huesos y pelvis. Era una nueva y amenazadora fase de la enfermedad que la ha perseguido durante mucho tanto tiempo. Pero cuando su oncólogo del Centro de Cáncer Sloan Kettering Memorial en Nueva York recomendó un ciclo de quimioterapia, ella se negó. Teixidor reconoce: "Me deprimió mucho la idea de tener que escoger entre la quimioterapia o nada".
A medida que su cáncer avanzaba, también lo había la ciencia. Una de las mutaciones de sus tumores ahora encajaba con un fármaco experimental que estaba siendo probado en el Centro de Cáncer Sloan Kettering Memorial y en otras partes. A pesar de que en ese momento los académicos debatían sobre el valor de la medicina de precisión para el cáncer (una reciente crítica científica la describió como "la ilusión de la precisión oncológica"), Teixidor decidió registrarse para participar en el ensayo clínico, y empezó a tomar el fármaco a finales de verano de 2015. En cuestión de semanas, empezó a notar cómo sus tumores disminuían, y las posteriores imágenes médicas confirmaron que efectivamente habían empezado a remitir.
A pesar de lo significativos que son este tipo de resultados, las dudas sobre la oncología de precisión mantienen preocupados a médicos, científicos, aseguradoras y a los más de 1,6 millones de estadounidenses que recibirán un diagnóstico de cáncer este año. ¿Cuántos pacientes podrían beneficiarse de la secuenciación del ADN de sus tumores? ¿Quién tendrá acceso a este enfoque médico, que resulta excepcionalmente caro? ¿Cuánto está la sociedad dispuesta a pagar para el pequeño subconjunto de pacientes que podría beneficiarse?
BUSCAR OBJETIVOS
Desde el Proyecto Genoma Humano, los científicos han soñado con disponer de información molecular precisa que guíe el diagnóstico y el tratamiento de las enfermedades humanas. La estrategia es: conocer la secuencia de ADN de la gente con determinadas enfermedades debería revelar las mutaciones que provocan las provocan y ofrecer objetivos claros para fármacos diseñados para atacarlos. Por desgracia, la complejidad biológica aún supera con creces a los conocimientos médicos. Aunque los investigadores esperaban que un número limitado de mutaciones comunes sirvieran para explicar un amplio abanico de enfermedades humanas (enfermedades cardiovasculares, hipertensión, diabetes, la esquizofrenia), no ha sido así.
A medida que su cáncer avanzaba, también lo había la ciencia.
Pero los tratamientos oncológicos ofrecen un rayo de luz en esta oscura historia. Los tumores suelen presentar aberraciones genéticas con varios objetivos en potencia para los fármacos. Mucho antes de que la oncología de precisión se popularizada, las terapias dirigidas habían ganado protagonismo en las clínicas de cáncer. En 1998, la Agencia de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) aprobó un fármaco para un subconjunto de pacientes de cáncer de mama cuyas células tumorales mostraban una versión especialmente hiperactiva de una molécula superficial, el receptor HER-2/neu. Herceptin fue el primer tratamiento dirigido contra el cáncer, y después llegaron otros dos fármacos superventas, Gleevec (que se dirigía a una mutación de una forma de leucemia) en 2001 y Zelboraf (diseñado contra a una mutación de melanomas) en 2011.
El éxito de estos fármacos aumentó la esperanza de que cuando la secuenciación de ADN fuera lo suficientemente barata y accesible, el genoma de cualquier tumor podría analizarse en busca de pistas para atacar directamente a sus mutaciones específicas. Eso, en resumidas cuentas, es la idea básica de la oncología de precisión: los médicos podrían realizar una biopsia del tumor, analizar su secuencia de ADN e identificar mutaciones, algunas de las cuales permitirían debilitar al cáncer gracias a fármacos moleculares ya aprobados. Antes los médicos luchaban por tratar el "cáncer de mama" o el "cáncer de piel", ahora sería la mutación y no el tejido de origen, la que definiría la enfermedad.
Suena casi irresistible. Pero los investigadores que creían que cada cáncer tenía un talón de Aquiles genético han descubierto que la biología de las mutaciones cancerígenas es mucho más complicada. De hecho, uno de los médicos de Carmen Teixidor ha estado en la vanguardia de demostrar lo realmente complicado que es.
UN CASO PERDIDO
En abril de 2012, médicos de 15 centros oncológicos líderes en Estados Unidos y Europa empezaron a registrar a sus pacientes en uno de los primeros grandes ensayos clínicos que iba utilizar la medicina de precisión contra el cáncer. El estudio se basó en conocimientos desarrollados a lo largo de la década anterior que demostraban que la mitad de todos los pacientes de melanoma, el mortífero cáncer de piel, poseían una alteración genética particular en un gen llamado BRAF. Esa mutación hacía que las células del melanoma fueran vulnerables al Zelboraf. El fármaco no era una cura, y ni siquiera era eficaz en todos los pacientes, pero en algunos de ellos sí logró frenar temporalmente la propagación de este cáncer tan maligno. Uno de los médicos de Teixidor del Centro de Cáncer Sloan Kettering Memorial David Hyman lideró un equipo internacional que buscaba la misma mutación en otros tipos de cáncer. Querían generar una "bolsa" de pacientes con la mutación, sin importar el tipo de cáncer que padecieran, para tratarlos con el fármaco.
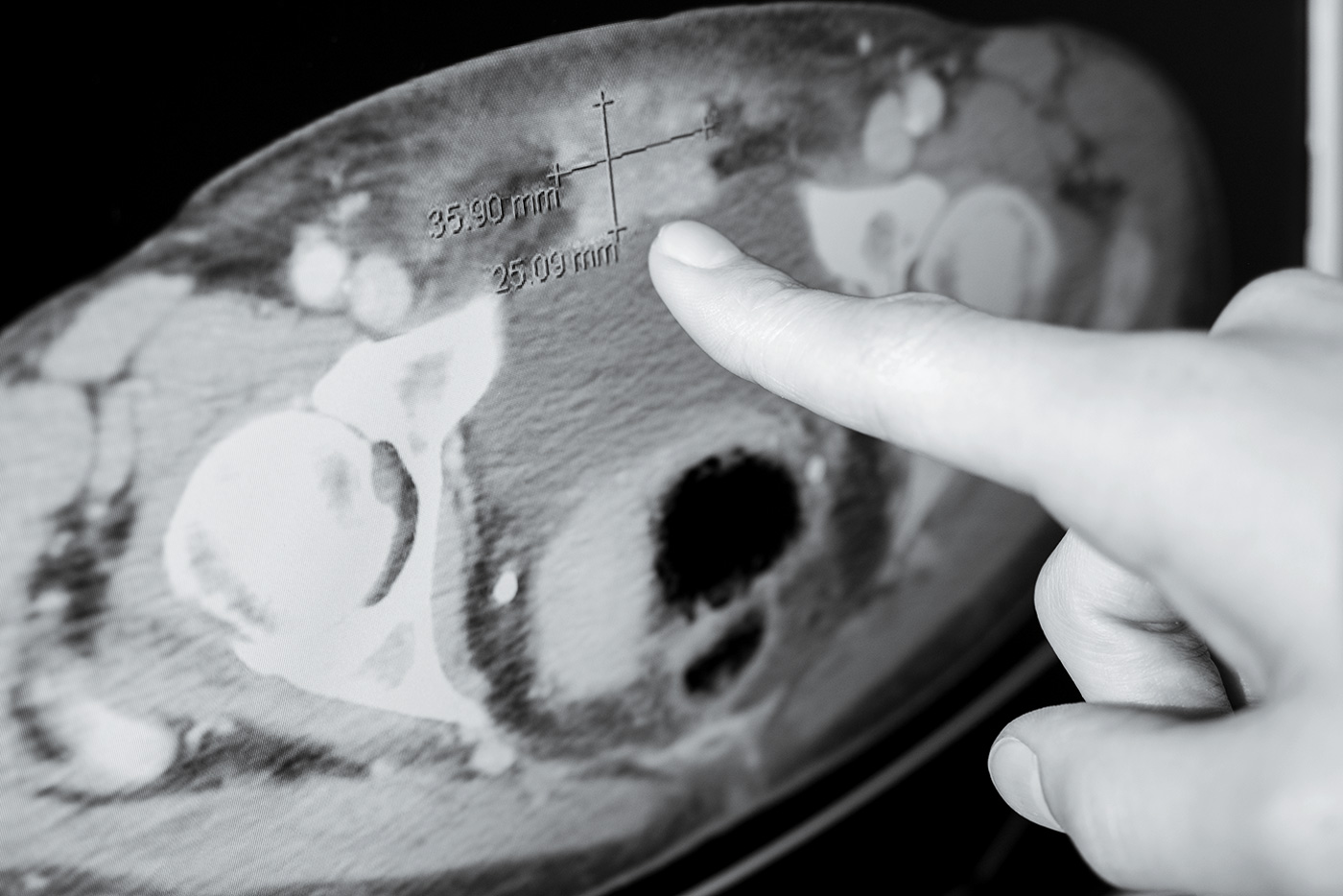
 Foto: Hyman de Sloan Kettering señala un tumor en una imagen de resonancia magnética. Crédito: Jonno Rattman.
Foto: Hyman de Sloan Kettering señala un tumor en una imagen de resonancia magnética. Crédito: Jonno Rattman.
Los resultados de aquel estudio, publicados en la revista New England Journal of Medicine en agosto de 2015, animaron a la comunidad ongológica pero también lanzaron una advertencia. Hyman y sus compañeros identificaron pacientes con la mutación BRAF que tenían cáncer de pulmón, cáncer de colon, cáncer de tiroides y otras formas de la enfermedad. En algunos casos, el fármaco funcionó; en otros casos, de forma algo sorprendente, no. En personas con cáncer de pulmón no microcítico, por ejemplo, el fármaco ralentizó la progresión de su enfermedad a más del 40% de los enfermos. Pero en pacientes de cáncer de colon que poseían la mutación idéntica, el fármaco no tuvo ningún efecto en absoluto.
 Foto: Un portaobjetos de microscopio que contiene tejido canceroso teñido de una biopsia. Crédito: Jonno Rattman.
Foto: Un portaobjetos de microscopio que contiene tejido canceroso teñido de una biopsia. Crédito: Jonno Rattman.
Este mensaje mixto preocupaba a oncólogos como el director nacional de Estrategia de Cuidados Gestionados de Flatiron Health, Michael Kolodziej, cuya empresa de análisis de datos intenta encontrar sentido en los mensajes de los historiales médicos electrónicos. Kolodziej advierte: "Siendo realistas, para muchos pacientes esto no será útil. Para otros, podría ser la cosa más importante que puedan hacer. Y ahora mismo no soy capaz de distinguir entre lo uno y lo otro".
Los dilemas como este abundan. La mayoría de las mutaciones cancerígenas detectadas son extremadamente raras, y la importancia médica de muchas de ellas se desconoce. Algunas mutaciones son tratables; otras no lo son, o al menos aún no. Además, los tratamientos no han tenido un éxito uniforme. Un subconjunto de pacientes responde, pero las respuestas suelen ser temporales, y otros muchos no responden en absoluto.
Ahora los investigadores intentan averiguar por qué. Más o menos cuando Hyman y sus compañeros publicaron sus resultados durante el verano de 2015, el Instituto Nacional del Cáncer de Estados Unidos (NCI, por sus siglas en inglés) lanzó un ambicioso estudio para probar la idea de emparejar una mutación específica, en cualquier tipo de cáncer, con una terapia dirigida apropiada. El estudio en curso incluye 24 subprotocolos distintos, de los cuales cada uno examina los cambios moleculares en una vía molecular a la que se dirigen los fármacos. El ensayo cuenta con más de 3.000 pacientes. El NCI gestiona la secuenciación de sus tumores, y cuando los investigadores identifican una correspondencia, lo que sucede alrededor del 22% de las veces, envía el fármaco apropiado directamente al centro del paciente.
"Creo que conseguiremos resolver este puzle, pero no será nada fácil"
Barbara Conley del NCI cree que parte del escepticismo frente a la oncología de precisión está justificado. La experta matiza: "Creo que conseguiremos resolver este puzle, Pero no será nada fácil". Hyman no le lleva la contraria. Pero señala que a medida que hay más tumores secuenciados y se desarrollan y prueban más fármacos dirigidos, la oncología de precisión está mejorando rápidamente. Un paciente en el lugar adecuado en el momento adecuado podría encontrar que una mutación que antes no era "terapéuticamente relevante" resulta ser tratable al día siguiente. Y con un golpe de teclado, Hyman ya puede encontrar a cualquier paciente en el sistema del Centro Sloan Kettering que posea cualquier mutación específica.
EL GANADOR DE LA LOTERÍA
En primavera de 2013, a Carmen Teixidor le realizaron una biopsia tumoral, pero cuando los investigadores del Centro Sloan Kettering buscaron en los lugares donde suelen aparecer las mutaciones cancerígenas (conocidos como puntos calientes), la prueba de secuenciación no funcionó. Repitieron la prueba el siguiente octubre, y esa vez los resultados demostraron que el ADN del tumor de Teixidor tenía varias mutaciones, incluida una en un gen llamado AKT1. Por desgracia, en ese momento no existía tratamiento. La mutación no era, según la jerga de medicina de precisión, "accionable". Pero al igual que otros pacientes del Centro Sloan Kettering, los datos del ADN de su tumor fueron introducidos en una base de datos accesible para el investigador principal de cualquier ensayo clínico del hospital que planeara probar un fármaco dirigido a cualquiera de sus mutaciones.
La mutación AKT fue identificada como causa de cáncer por primera vez en 2006, y varias farmacéuticas desarrollaron inhibidores de AKT. Los primeros ensayos con la población general de pacientes de cáncer fueron "sobre todo infructuosos", dice Hyman. Pero emparejar el fármaco con pacientes con la mutación vulnerable podría mejorar las probabilidades de una respuesta. Una de las empresas que trabajaba en inhibidores de AKT era AstraZeneca, que proporcionó un fármaco experimental llamado AZD5363 para un ensayo clínico en el Centro Sloan Kettering y otras clínicas. Cuando Hyman lanzó en el ensayo dirigido a AKT en 2014, el nombre de Carmen Teixidor le salió en la pantalla del ordenador. "Los progresos en la investigación consiguieron alcanzarla", recuerda Hyman.
 Foto: Un técnico de laboratorio devuelve muestras de ADN a un congelador de temperatura baja en el Centro de Cáncer Sloan Kettering Memorial. Crédito: Jonno Rattman.
Foto: Un técnico de laboratorio devuelve muestras de ADN a un congelador de temperatura baja en el Centro de Cáncer Sloan Kettering Memorial. Crédito: Jonno Rattman.
En septiembre de 2015, Teixidor empezó a tomar pastillas dirigidas a la mutación AKT de su cáncer, que avanzaba rápidamente. Al principio, experimentó efectos secundarios que la debilitaron, por lo que sus médicos ajustaron la dosis. Después, su respuesta fue tan rápida que los efectos fueron literalmente palpables. "Hubo resultados positivos prácticamente de inmediato", afirma. Tras varias semanas de tratamiento, recuerda, ya no notaba sus tumores. Hyman añade: "Desaparecieron. Es algo bastante típico cuando una terapia dirigida funciona. Funciona muy rápidamente".
Apenas dos meses después, los investigadores presentaron los resultados preliminares del ensayo de AKT en una reunión de la Asociación Estadounidense para las Investigaciones de Cáncer. Según Hyman, el mensaje era: "La mayoría de los pacientes han experimentado algún grado de regresión tumoral durante esta terapia". La respuesta de Teixidor, añadió, "ha sido especialmente duradera", y sus médicos ahora están estudiando la secuencia de ADN de sus células tumorales en busca de pistas acerca de por qué su cáncer ha sido especialmente sensible al tratamiento.
Durante una visita reciente al grupo de Hyman en el Centro Sloan Kettering, Teixidor se preguntó algo que pocos pacientes se planteaban sobre el fármaco experimental. La paciente recuerda: "Pregunté sobre los efectos secundarios a largo plazo". La respuesta: nadie lo sabe realmente.
¿MERECIÓ LA PENA?
Teixidor tuvo suerte de ser tratada en un importante centro académico. No todos los centros oncológicos tienen capacidad de aprovecharse de los últimos avances de la genómica tumoral. Esta desigualdad que fue reconocida recientemente por oficiales del proyecto Disparo a la Luna del Cáncer del presidente Obama. "La vasta mayoría de los estadounidenses no puede acceder fácilmente a pruebas de precisión para el cáncer", señalaron en un informe publicado en septiembre, "puesto que los ensayos clínicos oncológicos se realizan principalmente en grandes centros de investigación del cáncer y no en los centros comunitarios donde la mayoría de los pacientes reciben sus tratamientos".
 Foto: Un robot prepara muestras en un laboratorio en el Centro de Cáncer Sloan Kettering Memorial. Crédito: Jonno Rattman.
Foto: Un robot prepara muestras en un laboratorio en el Centro de Cáncer Sloan Kettering Memorial. Crédito: Jonno Rattman.
Efectivamente, la secuenciación de los tumores sigue siendo una práctica relativamente poco común. El antiguo director de los Institutos Nacionales de Salud de Estados Unidos y actual profesor de la Facultad de Medicina Weill Cornell (EEUU), Harold Varmus, dice que una de las grandes "oportunidades perdidas" de la genómica del cáncer es el bajo número de pacientes cuyos tumores son secuenciados. El programa federal Medicare no cubre este tipo de procedimiento, ni tampoco la mayoría de las aseguradoras privadas. El coste no despreciable: la secuenciación tumoral puede costar entre 560 y casi 950 euros por biopsia, en función de quién la practique. Pero Varmus señala que ya es más barata que algunas prestaciones básicas en los cuidados de cáncer, como múltiples pruebas de imágenes. "Estos pacientes pueden acabar haciéndose docenas de pruebas de imágenes (TAC, escáneres PET, resonancias magnéticas)", dice. Cada una de estas pruebas suele costar entre 470 euros y 4.700 euros.
 Foto: Las bases de datos del Centro de Cáncer Sloan Kettering Memorial significan que la información tumoral es fácilmente accesible. Crédito: Jonno Rattman.
Foto: Las bases de datos del Centro de Cáncer Sloan Kettering Memorial significan que la información tumoral es fácilmente accesible. Crédito: Jonno Rattman.
Pero el coste de las secuenciaciones solo son responsables de una parte del alto precio de la medicina de precisión oncológica. Las terapias dirigidas pueden costar fácilmente 9.500 euros al mes. Las aseguradoras no siempre las cubren, dada la incertidumbre respecto a cuántos pacientes se podrían beneficiar.
El oncólogo de la Universidad de Salud y Ciencia de Oregón en Portland (EEUU) Vinay Prasad calculó hace poco que tan sólo el 1,5% de los pacientes con tumores sólidos, recurrentes e intratables tendrían probabilidades de beneficiarse de terapias dirigidas, una estretegia que para muchos solo conseguiría alargar su supervivencia unos meses. A pesar del "bombo" que rodea los casos excepcionales en los que los pacientes responden de manera dramática, escribió en la revista Nature, "la mayoría de la gente que padece de cáncer no se beneficia de la estrategia de precisión". Otro oncólogo, Howard West del Instituto Sueco de Cáncer en Seattle (EEUU), cuestiona cómo los investigadores celebran "los pocos éxitos" sin "mencionar el denominador común de todos los pacientes tratados para lograr esos éxitos". Y añade, "Sí, hay unos pocos ganadores. Pero es igual que una lotería. ¿Merece la pena gastar millones en pruebas para encontrar a cuatro pacientes que de otro modo no se habrían encontrado?"
Estas críticas dejan perplejos a investigadores como Razelle Kurzrock del Centro de Cáncer Moores de la Universidad de California en San Diego (EEUU). Kurzrock y sus compañeros analizaron recientemente los resultados de cientos de ensayos clínicos. Según sus resultados, cuando los fármacos dirigidos se emparejan correctamente con mutaciones tumorales específicas, los pacientes tienen tasas de respuesta significativas y niveles más altos de supervivencia sin progresión. Este concepto hace referencia al tiempo transcurrido antes de que un cáncer se vuelva a progagar. "Claramente existe una gran mayoría de tipos de cáncer que responden", asegura.
Sus investigaciones, primero en el Centro de Cáncer MD Anderson en Houston (EEUU) y ahora en la Universidad de California en San Diego, sugieren que hay pacientes que ya se están beneficiando de la secuenciación de próxima generación y los fármacos emparejados. "Se pueden lograr respuestas estupendas", afirma, y añade que las tasas de respuesta han aumentado incluso más cuando los médicos emplean combinaciones de terapias dirigidas.
La esperanza es que cuando por fin haya más datos disponibles se pueda ayudar a un número de pacientes cada vez mayor. Hyman cita una alteración genética que suele aparecer en el 1% de los pacientes de cáncer de pulmón. El pasado mes de marzo, la FDA aprobó un fármaco que ha alargado "drásticamente" las vidas de estos pacientes, explica Hyman. Y afirma que no buscar esa mutación en los 225.000 estadounidenses diagnosticados con cáncer de pulmón cada año sería el equivalente a racionar los cuidados médicos.
Los médicos de Teixidor están estudiando la secuencia de ADN de sus células tumorales en busca de pistas.
Hyman defiende: "No podemos ignorarlo. Aunque no afecte al 100% de los pacientes, incluso si sirve para el 1% o para el 5% o el 10%, es [justificación] suficiente".
Sean cual sea el porcentaje, Carmen Teixidor se siente agradecida. Hace poco, un miércoles por la tarde se encontraba sentada delante de su ordenador revisando archivos digitales repletos de su arte. La artista explica que una serie actual de sus obras arranca con unas fotografías macro de 2,5 centímetros cuadrados de su propia piel. Teixidor modificó estas imágenes, "con arrugas y todo", al reproducirlas y manipularlas digitalmente para crear espectaculares telas y fantásticas formas tridimensionales como jarrones y flores.
 Foto: Teixidor sigue luchando contra su cáncer.
Foto: Teixidor sigue luchando contra su cáncer.
Crédito: Jonno Rattman.
Durante esa conversación, comentó que vivir con cáncer durante tanto tiempo la había liberado de algún modo. La paciente se preguntó: "¿Qué es la vida si no puedes sentir sus bordes?" Pero el pasado mes de noviembre los médicos le dijeron que su cáncer había empezado a crecer de nuevo, volviendo algo más incierto su futuro. Así que con una sonrisa triste, reconoce: "Ahora mismo preferiría no sentirlos".


